Salud├│ el Dr. Cubr├Łas a los asistentes, destacando la presencia entre ellos de algunos alumnos suyos. Felicit├│, asimismo, al equipo de Cien por Cien Natural por la organizaci├│n del evento y de todos los eventos y cursos que han organizado a lo largo de los a├▒os, destacando las dificultades que algo as├Ł comporta y la excelencia con que todos han sido organizados.
A continuaci├│n, antes de entrar en materia, el Dr. Cubr├Łas sorprendi├│ a los asistentes preguntando (y rogando sinceridad en la respuesta): ŌĆ£┬┐Qui├®nes nos vamos a dormir cuando empieza a oscurecer?, levanten la manoŌĆØ
El ponente empez├│ a contar manos alzadas, para considerar que eran muy pocos los presentes que se acostaban al oscurecer, y, sin embargo, biol├│gicamente hablando, todos deber├Łamos empezar a dormir cuando empieza a oscurecer, tal como se ha evidenciado desde el 2017, cuando se demostr├│ objetivamente el valor de los cronorritmos biol├│gicos, punto de partida de la cronofarmacolog├Ła o la cronofarmacia y la cronopatolog├Ła. ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗ
ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗ
Bien, ┬┐qu├® pasa en la tarde cuando ŌĆ£nosotros empezamos a oscurecerŌĆØ biol├│gicamente hablando?, pregunt├│ ret├│ricamente el ponente. A continuaci├│n, dio la respuesta.
Biol├│gicamente hablando la actividad enzim├Ītica baja, y de hecho no habr├Ła necesidad de cenar, incluso la cena muchas veces entorpece el efecto de detoxificaci├│n y limpieza anab├│lica asociada a la biolog├Ła humana.
Seguidamente, a modo ilustrativo, el ponente cont├│ una an├®cdota personal, declarando que no ten├Ła conflicto de intereses. Manifest├│ que su esposa y ├®l tomaban desde hac├Ła un mes un sobrecito de Caricol┬« todas las noches (y un d├Ła se encontraron disput├Īndose, y al final reparti├®ndose, un sobrecito). Coment├│ el Dr. Cubr├Łas que cenando tan tarde como se cena generalmente en nuestro pa├Łs, estamos sobrecargando la funci├│n y cargando la actividad enzim├Ītica nocturna, por eso la actividad enzim├Ītica de Caricol┬« ayuda a la digesti├│n y promueve un mejor descanso nocturno.
Entrando en materia. Disbiosis intestinal.
Abordando el tema de la disbiosis intestinal, el Dr. Cubr├Łas mencion├│ que se trata de un tema extremadamente interesante, pero que conviene abordar teniendo en cuenta que no se trata de algo est├Ītico y que desde el punto de vista cl├Łnico se tiende en los estudios a tratar desde un punto de vista cuasi convencional, similar al uso de antibi├│ticos, de forma exagerada y excesiva.
Record├│ el ponente que el impacto de la microbiota humana y el valor que tiene empez├│ a considerarse hace aproximadamente doce a├▒os, cuando se lleva a cabo el Proyecto del Microbioma Humano, al que se destinaron 230 millones de d├│lares por la FDA (Food and Drug Administration ŌĆō Agencia de alimentos y medicamentos) para investigar heces fecales, y hasta la fecha, sin lugar a dudas, ha dado muy buenos resultados en t├®rminos de conocimiento, encontrando una explicaci├│n biol├│gica a cosas que ya ten├Łamos por sabidas desde la medicina ancestral, como la ayurv├®dica y otras.
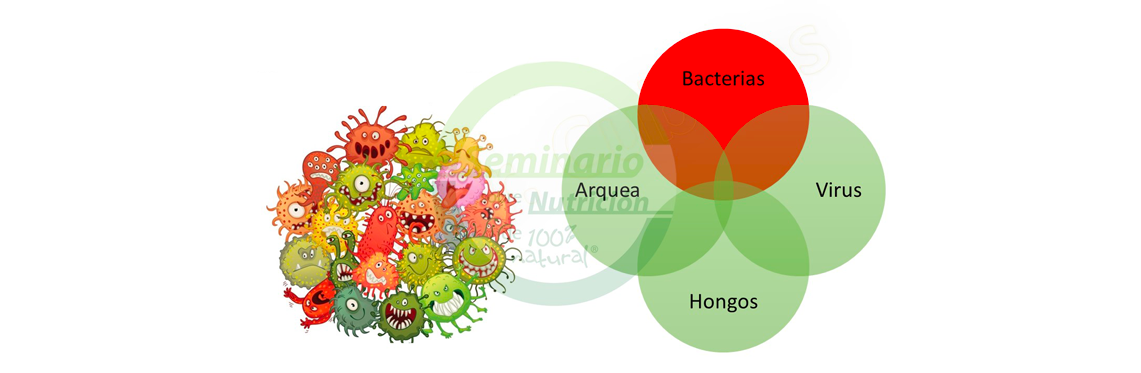
Si se hace un repaso conceptual al tema de la microbiota humana, hoy se sabe que est├Ī compuesta fundamental-mente por estos cuatro grupos de microorganismos:
bacterias, arqueas, virus y hongos, predominando las bacterias.
El n├║mero de bacterias que habitan en nuestro organismo es tan elevado que, ŌĆ£por cada c├®lula humana encontramos 9 bacteriasŌĆØ. Su conjunto puede llegar a pesar hasta 2 kilos. Alrededor de un 50% de la masa fecal se compone de bacterias. Estas bacterias pertenecen fundamentalmente a 4 filos: firmicutes, bacteroidetes, actinobacterias y proteobacterias.
Los dos primeros (firmicutes y bacteroidetes) tienen un rol crucial en el metabolismo humano. Manifest├│ el ponente que, llegados a este punto, cuando se estudia el microbioma y el microbiota, hay que prestar atenci├│n a una parte del concepto de las ciencias ├│micas que es muy importante, el metaboloma. No solo es importante saber qu├® grupos de bacterias hay en uno u otro lugar y su funci├│n, es asimismo importante saber qu├® metabolitos se producen secundariamente. Hoy en d├Ła la PCR cuantitativa en tiempo real con cebadores espec├Łficos basados en el gen 16S rRNA nos permite estudiar el microbiota intestinal, determinando la gen├│mica de las bacterias para poder ser mucho m├Īs objetivo en t├®rminos de emprender una labor terap├®utica.
Prosigui├│ el Dr. Cubr├Łas contextualizando el microbiota en el tubo digestivo, se├▒alando que hay una menor concentraci├│n a nivel g├Īstrico (101) que va aumentando hacia la parte distal: en el duodeno 103, en el yeyuno 104, en el ├Łleon 107 y en el colon 1012. Y tambi├®n cambian de manera din├Īmica los filos que encontramos en uno u otro lugar. A nivel g├Īstrico: Lactobacillus, Bellonella, Helicobacter; en duodeno, yeyuno e ├Łleon: Bacilli, Streptococcaceae, Actinobacteria, Actinomycinaeae, Corynebacteriaceae y en colon: Lachnospiraceae y Bacteroidetes, filos que son muy importantes y que tienen un rol crucial en la cl├Łnica del individuo. Por eso es importante que seamos capaces de conocer el microbiota, saber c├│mo funciona y cu├Īles son sus propiedades desde el punto de vista cl├Łnico.
Microbiota intestinal. Funciones
Pas├│ el Dr. Cubr├Łas a revisar las funciones del microbiota intestinal, destacando que desde el punto de vista cl├Łnico vale la pena advertir que el microbiota intestinal es la barrera n├║mero 1 en t├®rminos de detoxificaci├│n, en t├®rminos de control y de protecci├│n, de la salud del individuo. Y lo considera interesante porque generalmente, cuando se habla de mecanismos de detoxificaci├│n se suele considerar el h├Łgado como eje central, pero es importante percatarse que lo que ocurra a nivel hep├Ītico ocurre a nivel del enterocito y a nivel de la c├®lula pulmonar, es decir, que no se puede observar solo desde el punto de vista visceral. Sin lugar a dudas, es el microbiota intestinal la primera barrera, tiene funciones tr├│ficas interesantes, juega un rol crucial a nivel inmunitario, y hoy se empieza a saber con mayor profundidad que empieza a impactar de forma interesante en otra ├│mica que es la lipid├│mica, y diferentes se├▒alizaciones que dependen de estos grupos bacterianos y que optimizan o no el metabolismo de las grasas, modulando la lipog├®nesis y la oxidaci├│n de ├Īcidos grasos.

Asimismo, indic├│ el ponente que tambi├®n tiene una actividad metab├│lica crucial, que fue muy estudiada por el grupo de Gordon (1) hace unos a├▒os, demostrando que la ratio Bacteroidetes/Firmicutes juega un rol crucial, sobre todo en el componente metab├│lico. Y que existe un nexo crucial con el control de la inflamaci├│n (de la que se habl├│ por la ma├▒ana), que es fundamental controlar y manejar porque es una forma de poder amortiguar el impacto de tantas y tantas alteraciones a nivel multiorg├Īnico. Otros factores importantes, continu├│ el Dr. Cubr├Łas, son la s├Łntesis de vitaminas del complejo B y de la vitamina K, relacionada con las enfermedades cardiovasculares, as├Ł como el metabolismo de xenobi├│ticos y la regulaci├│n de la conducta del hu├®sped.

Disbiosis
Para hablar de disbiosis, coment├│ el Dr. Cubr├Łas, que se deb├Ła hablar de los ├Īcidos grasos de cadena corta, de microbioma versus microbiota, de sobrecrecimiento de g├®rmenes oportunistas, de permeabilidad intestinal (de la que dar├Ła solo una pincelada porque iba a haber una conferencia espec├Łfica sobre el tema, y del nexo entre el sistema nervioso central, el sistema nervioso l├Łmbico, el sistema nervioso aut├│nomo y el sistema nervioso ent├®rico (intestino como segundo cerebro). Tanto es as├Ł, qu├® si se hace una revisi├│n en PubMEd de lo publicado en el 2014, se encuentran un sinn├║mero de patolog├Łas ya estudiadas objetivamente que demuestran un nexo crucial, como un eje central de la disbiosis, y much├Łsimas de las patolog├Łas que m├Īs nos matan. Y el proyecto Microbioma Humano, es el que ha permitido acercarnos a entender qu├® es lo que pasa detr├Īs de estas alteraciones.

Indic├│ el ponente la dificultad de resumir en 50 minutos algo tan complejo, por lo que se centrar├Ī en los pilares de la disbiosis para hacer un resumen que ayude en el plano cl├Łnico.
Uno de los pilares cuando hay disbiosis intestinal, es la disfunci├│n del enterocito, esa c├®lula espectacular que tiene unas uniones proteicas estrechas, que permiten el paso selectivo de sustancias al torrente sangu├Łneo y que cuando se da├▒an dejan pasar elementos que fisiol├│gicamente no tendr├Łan por qu├® hacerlo. Por tanto, estamos hablando de permeabilidad intestinal asociada o leaky gut en ingl├®s, cuyo impacto se ha ido demostrando.
Los ├Īcidos grasos de cadena corta hay que revisarlos, continu├│ el ponente, pues nos podemos encontrar con g├®rmenes oportunistas que hayan sobrecrecido o no, y esto es muy importante. Se observa frecuentemente que llegan pacientes con Helicobacter pylori, Pseudomonas, Escherichia coli, Proteus mirabilisŌĆ” g├®rmenes propios que en cantidades suprafisiol├│gicas son patol├│gicos. Se utilizan m├║ltiples f├Īrmacos para intentar disminuir su concentraci├│n, pero si no se consigue llegar a la eubiosis no se va a lograr estabilizarlos, por ello en la labor asistencial se ve la alta tasa de recurrencia en pacientes con Helicobacter pylori tratados con triterapia farmacol├│gica, por ello hay que llegar a una eubiosis, hay que buscar la eubiosis y no pelear a golpe ├║nica y exclusivamente de f├Īrmacos.
A continuaci├│n, el Dr. Cubr├Łas, mencion├│ la importancia de los filos y se├▒al├│ como firmicutes, bacteroidetes y enzimas son importantes en cuanto a la inmunidad y a la parte metab├│lica. Y tambi├®n se deben considerar los par├Īsitos que a menudo no dan s├Łntomas cl├Łnicos gastrointestinales, pero si extraintestinales. Hay que valorar tambi├®n el microbiota nutritivo y el equilibrio entre el microbiota proteol├Łtico y el regulador. A├▒adi├│ el ponente, que cuando se empieza a hacer menci├│n del leaky gut y de la disbiosis intestinal, la causa principal no es la ingesta exagera de antibi├│ticos que tiene evidentemente su importancia, pero la causa n├║mero uno es el estr├®s, concretamente el distr├®s, no el eustr├®s que es fisiol├│gico y crea hormesis que nos permite ser m├Īs resistente y desarrollarnos a un modo de supervivencia, si no el distr├®s que es absolutamente patol├│gico.
Hablando de una manera llana, cuando hay permeabilidad intestinal y se rompen las uniones estrechas en vez de pasar un amino├Īcido llega a pasar un p├®ptido que tiene ochoŌĆ” doceŌĆ” amino├Īcidos y cuando llega al torrente sangu├Łneo es reconocido por el sistema inmune como un elemento literalmente extra├▒o, como un ant├Łgeno, y se forman complejos ant├Łgenos/anticuerpos que son literalmente demoledores porque se van a depositar donde encuentren una estructura molecular similar. Por ello, la tasa de patolog├Łas autoinmunes como hipotiroidismo autoinmune, psoriasis, lupus eritematoso sist├®mico, esclerosis m├║ltiple y, en general las enfermedades autoinmunes, est├Ī creciendo de forma tremenda. Esto tiene un nexo fundamental con las reacciones cruzadas que se producen secundariamente a la presencia de estos elementos inadecuados sobre los que debemos tener control.
Llegados a este punto, el Dr. Cubr├Łas brome├│ con la hora, ya que pasaban de las cinco de la tarde, hora en que ŌĆ£los niveles de cortisol de todo el mundo est├Īn downŌĆØ, raz├│n por la que ŌĆ£los ingleses trabajan nine to fiveŌĆØ comentando que al ponente le tocar├Ła mantener despierto al auditorio.
Se├▒alando la pantalla, fij├│ la atenci├│n de los asistentes en que el target n├║mero uno de la liberaci├│n de factor de necrosis tumoral alfa (TNF-alfa) es el enterocito contiguo, subrayando el rol fundamental que juega el que act├║a como un gatillo, para potenciar la expresi├│n cl├Łnica de muchas patolog├Łas que tocan el tubo digestivo.
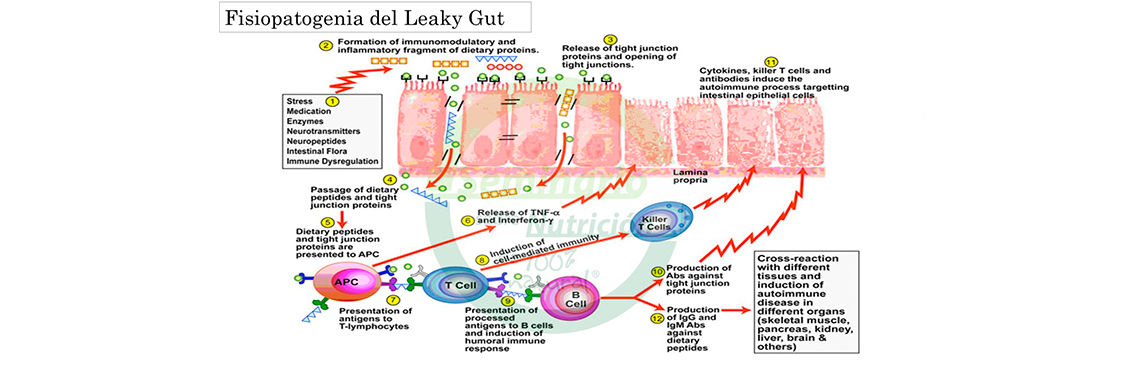
Referenci├│ el Dr. Cubr├Łas a su publicaci├│n ŌĆ£Los 13 jinetes del apocalipsis metab├│licaŌĆØ en el que se hace ├®nfasis en las alteraciones neuroendocrinas secundarias al estr├®s cr├│nico, porque estamos preparados para el estr├®s agudo, pero no para el cr├│nico. ŌĆ£El estr├®s agudo nos salva, el estr├®s cr├│nico nos mataŌĆØ, sentenci├│ el ponente. El estr├®s cr├│nico inflama, deteriora, oxida los ├Īcidos grasos poliinsaturados con dobles cadenas, con dobles enlaces (como el DHA) y cl├Łnicamente hablando se est├Īn recibiendo muchos pacientes con nivel de estr├®s oxidativo muy alto.
Pregunt├│ el ponente a los asistentes quienes en la sala med├Łan el estr├®s oxidativo de sus pacientes, se├▒alando su importancia ya que es necesario controlar el estr├®s oxidativo, y el proceso inflamatorio. Mencion├│ el Dr. Cubr├Łas el impacto sist├®mico de las alteraciones neuroendocrinas secundarias al estr├®s cr├│nico, de la permeabilidad intestinal y del microbiota obesog├®nico proinflamatorio y proarterioscler├│tico, o arterioscler├│tico. Y aclar├│ que dec├Ła proarterioscler├│tico porque de la microbiota depende la s├Łntesis de vitamina K, que produce la gamma-carboxilaci├│n de la osteocalcina (tambi├®n llamada bone Gla protein), que es importante para derivar el calcio al hueso y que llegue a adherirse a la trab├®cula de col├Īgeno del mismo, y que no acabe calcificando otros tejidos, resaltando que cada vez se ven m├Īs pacientes j├│venes con calcificaciones en los hombros o en las arterias, encontr├Īndose pacientes a los que se mide la rigidez arterial y presentan arterias con una arteriosclerosis que se corresponder├Ła con la de un paciente de 75 a├▒os. Y, a├▒adi├│, esto sucede porque ŌĆ£tenemos una tripa hecha polvoŌĆØ porque vivimos en distr├®s.
Segundo cerebro
Advirti├│ el Dr. Cubr├Łas que todav├Ła mucha gente (incluso colegas) se asustan cuando se les habla del intestino como segundo cerebro, pero realmente existe este segundo cerebro que tiene una relaci├│n directa y proporcional con el sistema nervioso aut├│nomo. Record├│ el ponente que el sistema nervioso aut├│nomo est├Ī conformado por el sistema nervioso simp├Ītico y por el sistema nervioso parasimp├Ītico, y que el neurotransmisor crucial del sistema simp├Ītico es la dopamina que, mencion├│, ŌĆ£es la madre de la noradrenalina para generar placer y la abuela de la adrenalina para generar agobio o estado de alertaŌĆØ.
Fisiol├│gicamente, en un medio biol├│gico y sano, el nexo entre dopamina, noradrenalina y adrenalina deber├Ła ceder un 70% de noradrenalina y un 30% de adrenalina, pero cuando se entra en situaci├│n de estr├®s, el porcentaje cambia y se deja de tener placer, y empieza el agobio sostenido en el tiempo. Esto constituye un problema serio porque, en general, nos estamos adaptando a vivir as├Ł y permanecemos en estado de alerta sin tener una causa justificada. Todo ello tiene un precio que se paga a nivel del sistema parasimp├Ītico y de su neurotransmisor m├Īs representativo, la acetilcolina, que act├║a sobre los receptores muscar├Łnicos y nicot├Łnicos, e influye en la memoria a corto plazo y en muchas funciones m├Īs. Puso como ejemplo el ponente que cuando las chicas se ponen nerviosas tienen necesidad frecuente de ir al ba├▒o porque tienen habitualmente un estado simp├Ītico adren├®rgico importante, con un parasimp├Ītico deteriorado. Lo que nos lleva a aprender que, si no somos capaces de conocer los puntos b├Īsicos del sistema l├Łmbico, tampoco seremos capaces de resolver una disbiosis intestinal.
Record├│ a continuaci├│n el Dr. Cubr├Łas, la fisiolog├Ła del sistema nervioso central y del sistema nervioso ent├®rico y la vinculaci├│n de los dos cerebros. Anim├│ el ponente a los asistentes a que digan tambi├®n a sus pacientes que en este segundo cerebro se han podido medir 500 millones de neuronas e identificar cuarenta neurotransmisores, entre los cuales un 50% de dopamina y hay estudios que muestran que hasta el 65% de la dopamina se sintetiza en el intestino, atraviesa la barrera hematoencef├Īlica y llega al sistema nervioso central, lo que se debe tener en cuenta, porque ŌĆ£entonces ya empezamos a ver que tenemos se├▒alizaciones inversas, aferentes y eferentes, y esto es muy importante en cl├ŁnicaŌĆØ. Adem├Īs, se produce el 95% de la serotonina que representa calma, sosiego, estabilidad, equilibrio.
Pas├│ a continuaci├│n a recordar asimismo la fisiolog├Ła de los plexos de Meissner (que se desarrolla en el intestino delgado y el colon principalmente, y se encarga de regular la digesti├│n y la absorci├│n en la mucosa y los vasos sangu├Łneos) y de Auerbach (que se encuentra en todo el tubo digestivo, y se encarga de coordinar la actividad de las capas musculares de dicho ├│rgano). Estamos hablando de los plexos que a trav├®s del nervio vago se comunican justamente con las neuronas sensoriales, motoras, las neuronas internas y la gl├Ła ent├®rica, esa gl├Ła ent├®rica que, desde el punto de vista anatomopatol├│gico, tiene una similitud extremadamente interesante con el sistema nervioso central en t├®rminos de gl├Ła y son una fotocopia literalmente una de la otra.
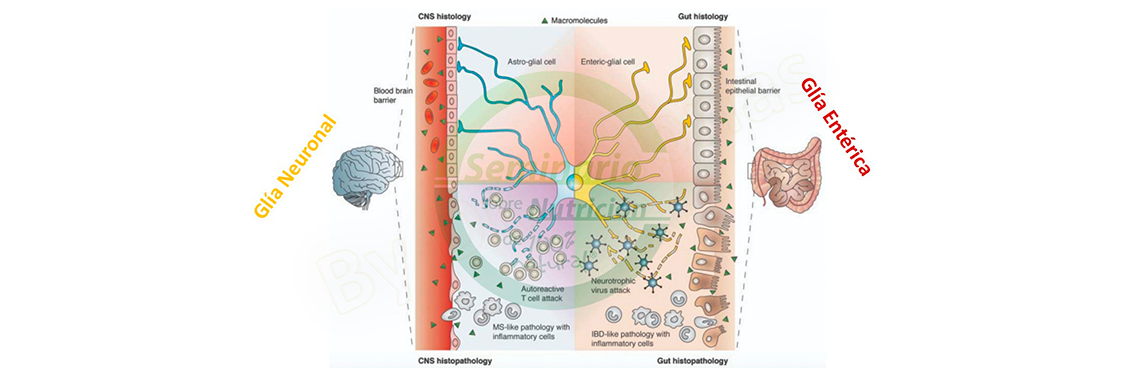
Fij├│ el Dr. Cubr├Łas la atenci├│n de los asistentes en el impacto crucial que el estr├®s y las emociones tienen en el tubo digestivo, a trav├®s del sistema l├Łmbico, mediante v├Łas aferentes y eferentes, o sea, enviando y recibiendo se├▒ales y en c├│mo, por ejemplo, la producci├│n de citocinas afecta al sistema nervioso central y, en este caso, al sistema nervioso aut├│nomo, y c├│mo el nervio vago ayuda a controlar los plexos de Meissner y de Auerbach en el tubo digestivo.
Tambi├®n llam├│ la atenci├│n en c├│mo, en t├®rminos sobre todo de control del sue├▒o, depende en gran medida del microbiota, debido a que hay microbiota productor de GABA (├Īcido ╬│-aminobut├Łrico), que es un neurotransmisor inhibitorio por excelencia, y en c├│mo luego aparece lo contrario, o sea, el impulso desde el sistema nervioso ent├®rico hacia la actividad adren├®rgica y no adren├®rgica en el tubo digestivo que produce una alteraci├│n del microbiota. Actualmente en lo que a la salud del microbiota se refiere hay dos problemas que se suman, el alto consumo de antibi├│ticos y el estr├®s con un mayor n├║mero de estresados que de consumo de antibi├│ticos.
A├▒adi├│ el Dr. Cubr├Łas que, aunque el tema seguro que se va a desarrollar por otros ponentes, no quer├Ła dejar de mencionar que la medicina del siglo XXI (nombre por cierto del Congreso de SENMO que se celebr├│ en Madrid del 5 al 7 de marzo de 2020) contempla el nexo crucial directo y proporcional entre permeabilidad intestinal y permeabilidad de la barrera encef├Īlica y, tambi├®n subrayar c├│mo se est├Īn viendo translocaciones importantes de procesos inflamatorios en el sistema nervioso central, neuroinflamaci├│n, causada por problemas digestivos, y esto es sumamente importante y puede estar detr├Īs del entendimiento de los pacientes con esclerosis m├║ltiple, incluso los pacientes con esclerosis lateral amiotr├│fica o enfermedad de Lou Gehrig.
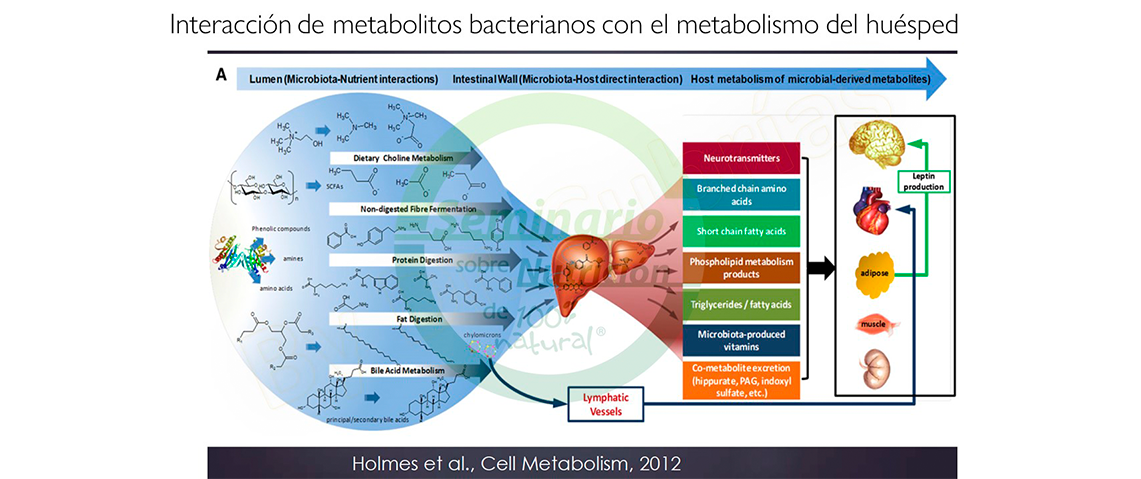
Interacci├│n de metabolitos bacterianos con el metabolismo del hu├®sped
Se├▒al├│ el ponente la importancia de la interacci├│n de los metabolitos bacterianos con el metabolismo del hu├®sped y recomend├│ la lectura del trabajo de Holmes et al de 2012 (2), sobre la importancia de la composici├│n y actividad de la microbiota intestinal en relaci├│n con el fenotipo metab├│lico del hu├®sped y el riesgo de enfermedad y, asimismo, destac├│ que incluso nuestro comportamiento, nuestro estado de ├Īnimo, nuestro control de la insulinosensibilidad, tiene que ver directamente con los neurop├®ptidos que tienen relaciones cruciales con los niveles de ├Īcidos grasos de cadena corta que dependen de nuestra microbiota.
Tambi├®n invit├│ al auditorio a reparar en el impacto que tiene la hipercortisolemia de un individuo en un estado suprafisiol├│gico. Record├│ el Dr. Cubr├Łas que el cortisol es absolutamente fisiol├│gico, pero que cualquier estado de hipercortisolemia por encima del nivel fisiol├│gico, va a producir un desequilibrio entre los neurotransmisores y conlleva importantes alteraciones neuroendocrinas asociadas al estr├®s cr├│nico. Lo normal es que cuando los niveles de cortisol est├®n altos se inhiba la producci├│n de ACTH, la adrenocorticotropa, para que no aumente la se├▒alizaci├│n sobre la corteza suprarrenal y se produzca m├Īs cortisol, pero esa capacidad se pierde con el estr├®s cr├│nico, en el que se mantiene un nivel suprafisiol├│gico constantemente lo que, evidentemente, sabemos que es proinflamatorio y que genera un deterioro crucial.
Expuso el ponente a continuaci├│n, la importancia que tiene desde el punto de vista cl├Łnico un concepto nuevo, el metaboloma. Se trata de una ciencia ├│mica muy interesante que nos permite conocer cu├Īles son los metabolitos que se pueden generar secundariamente a lo que ingerimos, aunque a veces no sabemos si guardan relaci├│n con una cl├Łnica espec├Łfica, una alteraci├│n de microbiota no siempre significa que haya metabolitos propatol├│gicos, pero en la medida que se estudia el microbiota deber├Łan estudiarse los metabolitos org├Īnicos, que son un dato importante para saber lo que est├Ī pasando.
Seguidamente, pas├│ a considerar el papel de los ├Īcidos grasos de cadena corta que son grandes moduladores de la respuesta inflamatoria. Los ├Īcidos grasos de cadena corta intervienen en la activaci├│n del inflamasoma (complejo multiproteico responsable de la activaci├│n de los procesos inflamatorios). Si se produce una alteraci├│n de los ├Īcidos grasos de cadena corta se producen alteraciones del inflamasoma, multiplicando el efecto inflamatorio, y ŌĆ£recuerden una cosa conceptual, detr├Īs de una inflamaci├│n no resuelta hay siempre, siempre, siempre, estr├®s oxidativoŌĆØ advirti├│ el ponente. Y los que se oxidan son los ├Īcidos grasos con dobles cadenas, los poliinsaturados que dan permeabilidad a la membrana y muchas enfermedades como el hipotiroidismo entre otras, est├Ī coligado secundariamente a una rigidez importante de membrana asociado a niveles de ├Īcidos grasos poliinsaturados de cadena larga muy deteriorados o muy inadecuados para la salud de cualquier individuo. Record├│ en este punto la relaci├│n entre neuroinflamaci├│n, activaci├│n de la gl├Ła y activaci├│n del inflamasoma.
Semiolog├Ła Cl├Łnica de Disbiosis Intestinal
Pidi├│ el Dr. Cubr├Łas a los asistentes que levantaran la mano qui├®nes no tuvieran distensi├│n abdominal a lo largo del d├Ła, luego quienes amanec├Łan con el abdomen plano y sufr├Łan durante el d├Ła distensi├│n abdominal y gases, quienes tuvieran aerofagia, c├│licos abdominales, gases f├®tidos, sobre todo tras la ingesta de una sobrecarga proteica, quienes tuvieran deseos de dulces y el chocolate vespertino y qui├®nes tuvieran alteraciones del h├Ībito defecatorio, diarrea versus estre├▒imiento. Se├▒alando la importancia de trasladar esta pregunta a los pacientes y a├▒adir un 5% de estr├®s a la cantidad de s├Łntomas que van a emanar de estas preguntas y que conducen al concepto conocido como neurodiston├Ła vegetativa, que se corresponde con un umbral de estr├®s deteriorado que se dispara al menor estr├®s a├▒adido y lleva a somatizar.


Relacion├│ a continuaci├│n otros s├Łntomas como: alteraciones del humor sin causa aparente; memoria reciente alterada, incluso en j├│venes de 25-30 a├▒os (cosa que antes no se ve├Ła y que viene relacionado con un gasto de acetilcolina); irascibilidad; alteraciones del sue├▒o intermedio y conciliaci├│n, que a menudo no responden o dejan de responder r├Īpidamente a tratamientos farmacol├│gicos; fatiga, dolor osteomuscular, cefalea tensional, agudizaci├│n de las migra├▒as (atenci├│n a las migra├▒as digestivas); erupci├│n, colitis, enteritis, acn├® adulto (por disbiosis intestinal con s├Łndrome de dominancia estrog├®nica que depende de la microbiota gracias a la betaglucuronidasa que reabsorbe muchos estr├│genos y que sobrecarga la funci├│n hep├Ītica) y autoinmunidad con target neurol├│gico.
Llegados a este punto, el ponente proyect├│ un video ilustrativo con datos interesantes que anexan el tema del tubo digestivo con la g├®nesis del c├Īncer. Asimismo, mostr├│ varios estudios publicados (Vivarelli et al. 2019 (3); Nagano et al. 2019 (4); Carding et al. 2015 (5)).
Estos estudios muestran objetivamente diferentes filos asociados con el efecto antitumoral y otros filos asociados con el efecto protumoral, absolutamente estudiado y objetivamente demostrado; en el de Vivarelli el al (3), se muestra los efectos y las v├Łas por las cuales se han estudiado y c├│mo las bacterias pat├│genas intestinales tambi├®n pueden interferir con la respuesta al da├▒o del ADN y reparar las v├Łas, como en el caso de Shigella flexneri, induciendo la degradaci├│n de p53 de las c├®lulas del hu├®sped, lo que aumenta la probabilidad de introducir mutaciones durante la respuesta al da├▒o del ADN en c├®lulas infectadas, y la implicaci├│n de diversas cepas bacterianas en la activaci├│n de la v├Ła beta-catenina. Todos estos conocimientos estudiados en cuanto al microbiota, constituyen un target nuevo en el ├Īmbito del manejo del paciente neopl├Īsico. Recomend├│ tambi├®n el ponente la lectura del estudio de Carding et al. 2015 (5), porque habla de la cantidad de patolog├Łas que se pueden anexar a las interacciones del tubo digestivo, que ya hab├Ła sido abordado en su mencionado libro ŌĆ£Los trece jinetes del Apocalipsis Metab├│licaŌĆØ (2016-2017). Y es sumamente importante tener en cuenta, que hay enfermedades cardiovasculares que est├Īn asociadas a las alteraciones del microbiota intestinal.
Lament├│ el Dr. Cubr├Łas no tener tiempo para abundar en otras interesantes consideraciones. Como el papel de los LPS (lipopolisac├Īridos) bacterianos relacionados con una respuesta inflamatoria intensa en el estado endotox├®mico secundario a la disbiosis intestinal, que hace qu├® afecte a m├║ltiples ├│rganos. Y algo m├Īs que importante, qu├® son las alteraciones del microbiota y la cronodisrupci├│n, y la influencia tanto en v├Ła aferente como eferente; hay alteraciones del microbiota que condicionan negativamente nuestros cronorritmos, y las alteraciones de los cronorritmos multiplican el da├▒o que existe a nivel del microbiota (6).
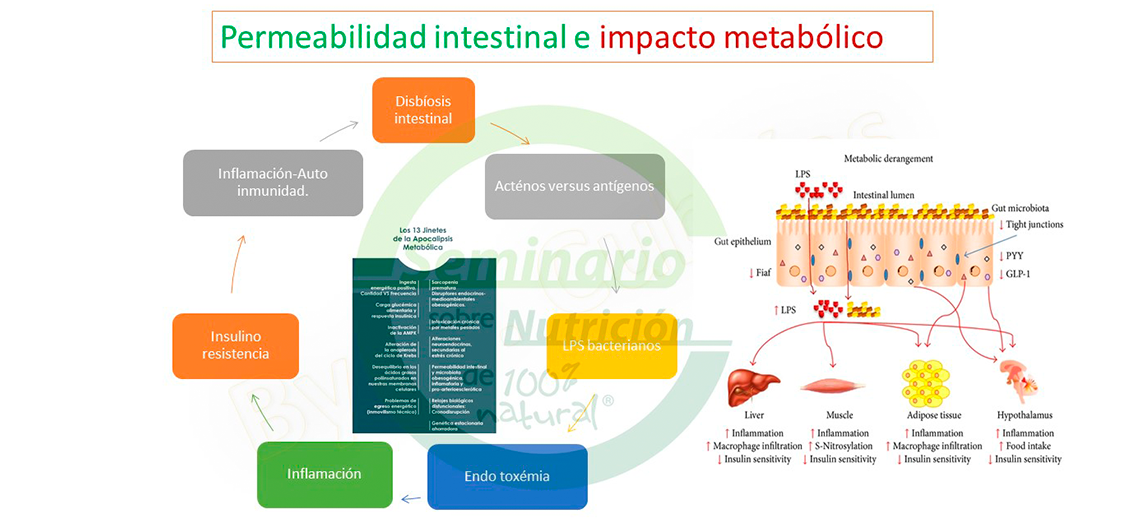
Tambi├®n volvi├│ a incidir el ponente en que, a menudo, la causa fundamental de patolog├Ła arterioscler├│tica tiene que ver con el d├®ficit de vitamina K2 tan necesaria para la ╬│-carboxilaci├│n de la osteocalcina y grantizar que el calcio se deposite en el entramado que existe de col├Īgeno a nivel ├│seo, como ya hab├Ła mencionado (7,8,9).
Por otro lado, record├│ el Dr. Cubr├Łas que la disbiosis intestinal, siempre ha sido importante como un eje central que permite entender los nexos que hay desde el punto de vista fisiopatog├®nico en t├®rminos metab├│licos, como la generaci├│n de la insulinorresistencia y la inflamaci├│n en un estado potencial tal como ocurre a trav├®s del inflamasoma. Record├│ los estudios de Gordon (1) que demostraron que en ratones ax├®nicos (libres de g├®rmenes) se requer├Ła casi un 30% m├Īs de aporte energ├®tico por alteraci├│n de la microbiota que en ratones no ax├®nicos y como el ratio Bacteroidetes/Firmicutes, es importante en relaci├│n con la obesidad, ya que una alteraci├│n con una mayor proporci├│n de Firmicuetes determina una mayor capacidad de extraer energ├Ła de fibra no digerible, de la que te├│ricamente no deber├Łamos extraer energ├Ła y eso conlleva una aumento de peso. Ejemplific├│ el ponente con el caso del paciente que llega a la consulta con aumento de peso y dice que no come m├Īs que lechuga y no le creemos, pero es cierto, sucede que ese paciente tiene un microbiota muy complicado en t├®rminos cl├Łnicos.
Integrando el alcance patol├│gico de la permeabilidad intestinal
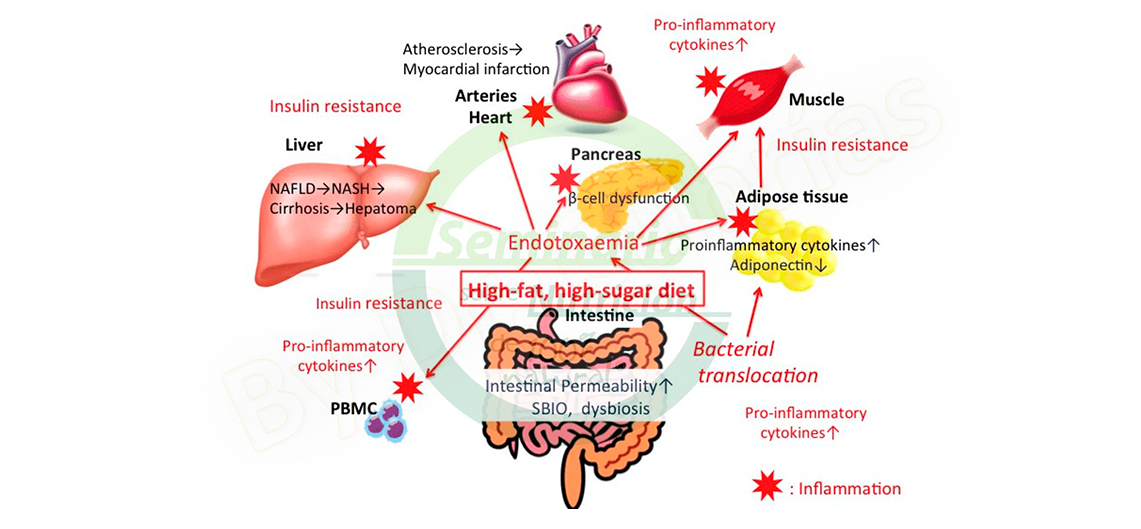
Explic├│ el Dr. Cubr├Łas, que una mala alimentaci├│n lleva a la permeabilidad intestinal, la inflamaci├│n y la disbiosis, con consecuencias nefastas sobre distintos sistemas, desde la arteriosclerosis que se ha comentado hasta el c├Īncer. Por lo tanto, para ser consecuentes se debe promover una alimentaci├│n saludable, con niveles adecuados de fibra y de grasas saludables, que fomente una buena microbiota, que disminuya la permeabilidad intestinal, la inflamaci├│n, la insulinorresistencia, que aumente la sensibilidad, y que disminuya el riesgo cardiovascular.
Hay mucho donde aprender, pronunci├│ el ponente y recomend├│ a continuaci├│n la lectura del estudio de Carding (2016) (5), a su juicio muy interesante, porque muestra todo el nexo entre la disbiosis intestinal estudiada hasta la fecha. Abund├│ de nuevo en el inter├®s de la metagen├│mica, que permite determinar la composici├│n de los microorganismos presentes e identificar las bacterias activas mediante la secuenciaci├│n del gen ADNr 16S. El estudio de los metabolitos en orina permite detectar marcadores de disbiosis espec├Łficos de microorganismos. El metaboloma es muy importante porque nos indica realmente lo que se est├Ī produciendo. Mostr├│ el ponente los resultados de algunos casos y c├│mo desde el punto de vista cl├Łnico, hay marcadores que pueden objetivar, por ejemplo, un aumento de paracresol que puede indicar sobrecrecimiento de Clostridium difficile, que tiene la capacidad de producirlo y a nivel neuronal el para-cresol inhibe la dopamina beta hidroxilasa, que es la enzima que convierte la dopamina en norepinefrina para convertirse luego en epinefrina, y si esto ocurre y el ratio homovan├Łlico/vanilmand├®lico se dispara (record├│ el Dr. Cubr├Łas lo que sucede en el caso de feocromocitoma), se genera un estado de neuroexcitaci├│n que genera una dificultad imperiosa para concentrarse. Esto est├Ī detr├Īs de lo que ocurre con muchos ni├▒itos nuestros que tienen trastornos del espectro autista. Esto est├Ī detr├Īs de muchos pacientes nuestros adultos que tienen dificultad para concentrarse, a├▒adi├│ el ponente.
As├Ł pues, una medicina moderna debe considerar que los neurotransmisores nos tienen que ayudar a entender lo que pasa en el tubo digestivo, y lo que sucede en el tubo digestivo nos tiene que ayudar a entender lo que est├Ī pasando a nivel del sistema nervioso central.
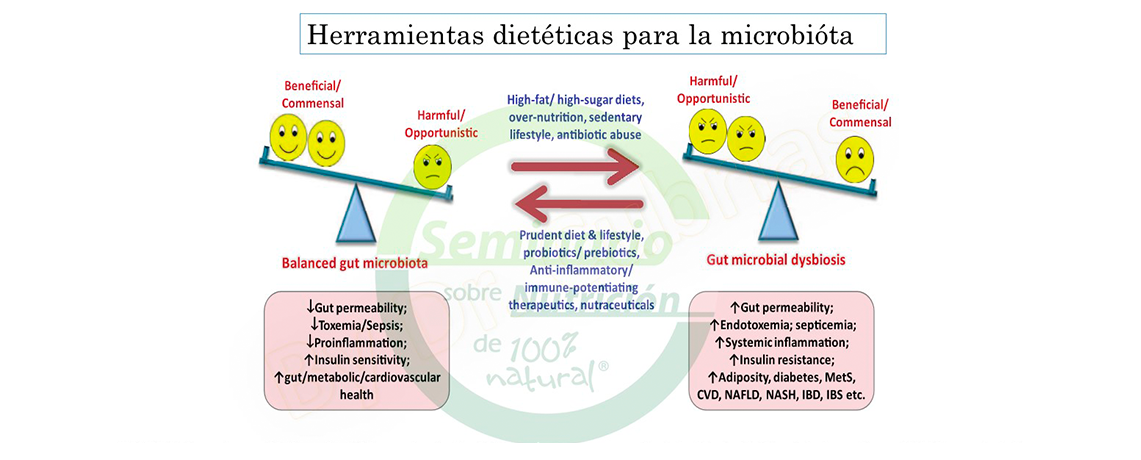
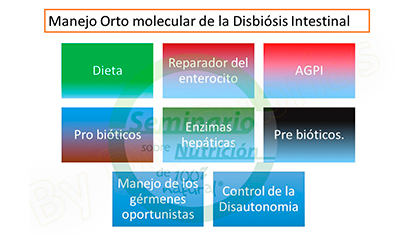
Manejo ortomolecular de la disbiosis intestinal
Para el manejo ortomolecular, el Dr. Cubr├Łas indic├│ que se debe establecer dieta reparadora de enterocitos, con ├Īcidos grasos poliinsaturados, probi├│ticos adecuados en el momento adecuado, enzimas hep├Īticas muchas veces muy importantes, prebi├│ticos en el momento adecuado, manejo de los g├®rmenes oportunistas, y control de la disautonom├Ła.
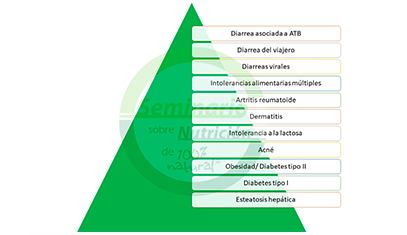
 ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗSi no se controla el eje del sistema nervioso simp├Ītico/parasimp├Ītico no se va a curar nunca una disbiosis y se cronifica el cuadro. Indic├│ el ponente la importancia de la utilizaci├│n de los probi├│ticos como armas terap├®uticas, aunque indic├│ que no lo iba a desarrollar, dado que iba a haber una ponencia espec├Łfica sobre el tema. Mostr├│ dos cuadros en los que se ve├Łan diversas enfermedades asociadas que pod├Łan ser tratadas con probi├│ticos como diarreas, intolerancias alimentarias, enfermedades inmunes y al├®rgicas, obesidad, diabetes, esteatosis o acn├®, pero tambi├®n: depresiones, bipolaridad, menopausia y enfermedades del tracto digestivo, entre otras.
ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗSi no se controla el eje del sistema nervioso simp├Ītico/parasimp├Ītico no se va a curar nunca una disbiosis y se cronifica el cuadro. Indic├│ el ponente la importancia de la utilizaci├│n de los probi├│ticos como armas terap├®uticas, aunque indic├│ que no lo iba a desarrollar, dado que iba a haber una ponencia espec├Łfica sobre el tema. Mostr├│ dos cuadros en los que se ve├Łan diversas enfermedades asociadas que pod├Łan ser tratadas con probi├│ticos como diarreas, intolerancias alimentarias, enfermedades inmunes y al├®rgicas, obesidad, diabetes, esteatosis o acn├®, pero tambi├®n: depresiones, bipolaridad, menopausia y enfermedades del tracto digestivo, entre otras.
Para finalizar, el Dr. Cubr├Łas, habl├│ de los datos que hoy se conocen sobre como la alimentaci├│n parenteral dirigida al microbiota intestinal fomenta su capacidad de mejorar el microbiota y la capacidad de recuperaci├│n del intestino (10).
Nombr├│ a continuaci├│n el ponente, varias herramientas biol├│gicas y farmacol├│gicas, muy interesantes, que dar├Łan, dijo, para una ponencia completa.
 ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗEntre ellas substancias como la glutamina, que alimenta el enterocito; la c├║rcuma y la quercetina que son reguladoras de la respuesta inflamatoria. El EPA y el DHA, de los que ya se habl├│ durante la ma├▒ana; el ├Īcido gamma-linol├®nico que es crucial para la producci├│n de prostaglandinas antiinflamatorias, PGE1, PGE3; el palmitoleico u omega-7, de gran y creciente inter├®s; los antibacterianos y los antiparasitarios. Y tambi├®n los prebi├│ticos y probi├│ticos, que se tratar├Īn como se ha mencionado en una ponencia espec├Łfica, las enzimas, y sin lugar a dudas los adapt├│genos porque, subrayo el ponente, tenemos una pandemia de disbiosis intestinal, tenemos una pandemia de pacientes con, literalmente, dificultad para mantener un estado de autonom├Ła, tienen disautonom├Ła, y la disautonom├Ła dopamino-adren├®rgica, que lo vemos cada d├Ła por ah├Ł, m├Īs frecuente de lo que imaginamos, si no utilizamos adapt├│genos con estos individuos, no vamos a disminuir el impacto que tiene la misma, no solamente en el tubo digestivo, sino a nivel sist├®mico. Entonces, se convierte en una herramienta sumamente importante.
ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗEntre ellas substancias como la glutamina, que alimenta el enterocito; la c├║rcuma y la quercetina que son reguladoras de la respuesta inflamatoria. El EPA y el DHA, de los que ya se habl├│ durante la ma├▒ana; el ├Īcido gamma-linol├®nico que es crucial para la producci├│n de prostaglandinas antiinflamatorias, PGE1, PGE3; el palmitoleico u omega-7, de gran y creciente inter├®s; los antibacterianos y los antiparasitarios. Y tambi├®n los prebi├│ticos y probi├│ticos, que se tratar├Īn como se ha mencionado en una ponencia espec├Łfica, las enzimas, y sin lugar a dudas los adapt├│genos porque, subrayo el ponente, tenemos una pandemia de disbiosis intestinal, tenemos una pandemia de pacientes con, literalmente, dificultad para mantener un estado de autonom├Ła, tienen disautonom├Ła, y la disautonom├Ła dopamino-adren├®rgica, que lo vemos cada d├Ła por ah├Ł, m├Īs frecuente de lo que imaginamos, si no utilizamos adapt├│genos con estos individuos, no vamos a disminuir el impacto que tiene la misma, no solamente en el tubo digestivo, sino a nivel sist├®mico. Entonces, se convierte en una herramienta sumamente importante.
Mencion├│ tambi├®n el ponente, los ├Īcidos but├Łrico y propanoico o propi├│nico, que pueden aportar beneficio en pacientes con patolog├Łas como la esclerosis m├║ltiple. Asimo, la necesidad absoluta de controlar el cronorritmo.
- Gordon, Jeffrey I. es miembro del Center for Gut Microbiome and Nutrition Research, Washington University School of Medicine, St. Louis, MO 63110, USA y del Department of Biochemistry and Molecular Biophysics, Washington University School of Medicine, St. Louis, MO 63110, USA, ha liderado y participado en muchos estudios sobre microbiota que se pueden encontrar relacionados en PubMed. Se aconseja la lectura de la publicaci├│n: Lozupone CA, Stombaugh JI, Gordon JI, Jansson JK, Knight R. Diversity, stability and resilience of the human gut microbiota. Nature. 2012;489(7415):220ŌĆÉ230. doi:10.1038/nature11550 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3577372/pdf/nihms442625.pdf.
- Holmes E, Li JV, Marchesi JR, Nicholson JK. Gut microbiota composition and activity in relation to host metabolic phenotype and disease risk. Cell Metab. 2012;16(5):559ŌĆō564. doi:10.1016/j.cmet.2012.10.007
- Vivarelli S, Salemi R, Candido S, et al. Gut Microbiota and Cancer: From Pathogenesis to Therapy. Cancers (Basel). 2019;11(1):38. Published 2019 Jan 3. doi:10.3390/cancers11010038
- Nagano T, Otoshi T, Hazama D, et al. Novel cancer therapy targeting microbiome. Onco Targets Ther. 2019;12:3619ŌĆÉ3624. Published 2019 May 13. doi:10.2147/OTT.S207546
- Carding S, Verbeke K, Vipond DT, Corfe BM, Owen LJ. Dysbiosis of the gut microbiota in disease. Microb Ecol Health Dis. 2015;26:26191. Published 2015 Feb 2. doi:10.3402/mehd.v26.26191
- Parkar SG, Kalsbeek A, Cheeseman JF. Potential Role for the Gut Microbiota in Modulating Host Circadian Rhythms and Metabolic Health. Microorganisms. 2019;7(2):41. Published 2019 Jan 31. doi:10.3390/microorganisms7020041
- D├Łaz Curiel M.. Acci├│n de la vitamina K sobre la salud ├│sea. Rev Osteoporos Metab Miner [Internet]. 2015 Mar [citado 2020 Mayo 02] ; 7( 1 ): 33-38. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1889-836X2015000100008&lng=es. http://dx.doi.org/10.4321/S1889-836X2015000100008.
- Hauschka PV, Lian JB, Cole DE, Gundberg CM. Osteocalcin and matrix Gla protein: vitamin K-dependent proteins in bone. Physiol Rev. 1989;69(3):990ŌĆÉ1047. doi:10.1152/physrev.1989.69.3.990
- Siraki M, Tsugawa N, Okano T. Recent advances in vitamin K-dependent Gla-containing proteins and vitamin K nutrition. Osteoporosis and Sarcopenia.Volume 1, Issue 1, September 2015, Pages 22-38. https://www.sciencedirect.com/science/article/pii/S2405525515000102
- Shah R, Kellermayer R. Microbiome associations of therapeutic enteral nutrition. Nutrients. 2014;6(11):5298ŌĆÉ5311. Published 2014 Nov 21. doi:10.3390/nu6115298
1 Producto a base de enzimas de pulpa de papaya ecol├│gica de Cien por Cien Natural.
2 Reacci├│n en cadena de la Polimerasa
3 El gen 16S rRNA se utiliza para estudios filogen├®ticos ya que su secuencia est├Ī altamente conservada entre las distintas especies de bacterias y arqueas
Resumen preparado por la Prof.┬¬ M┬¬ Jos├® Alonso como moderadora de la VIII Edici├│n del Seminario sobre Nutrici├│n del 22 de febrero de 2020 en Barcelona, donde tuvo lugar la ponencia del Dr. Jorge L. Cubr├Łas.
Dr. Jorge L. Cubr├Łas
M├®dico cl├Łnico con posgrado en patolog├Łas Cardiometab├│licas y Vasculares, ha tenido la siguiente trayectoria profesional:
- Doctor en Ciencias M├®dicas por la Universidad de las Villas en Cuba
- M├®dico Cirujano por la Universidad de Chile
- Licenciado en Medicina por el MEC, Espa├▒a
- Formado en Bioqu├Łmica Cl├Łnica, en el Instituto del Metabolismo Celular, Espa├▒a.
- Formado por el Profesor Efra├Łn Olszewer en Medicina Ortomolecular, FAPES, Brasil.
- Especialista en medicina anti envejecimiento por la Universidad de Sevilla, Espa├▒a.
- Co fundador de la Sociedad espa├▒ola de nutrici├│n y medicina ortomolecular, SENMO
- Docente en varias diplomaturas universitarias en Espa├▒a.
- Conferencista nacional e internacional en los ├║ltimos 14 a├▒os.
- Ha escritos varios art├Łculos para libros en materia de metabolismo energ├®tico.
- Experiencia hospitalaria y extra hospitalaria en los ├║ltimos 23 a├▒os con m├Īs de 20.000 pacientes vistos en el ├Īmbito de la pr├Īctica cl├Łnica y ortomolecular.
- Co-creador y gestor de congresos internacionales en materia de medicina y nutrici├│n ortomolecular en Espa├▒a.
- Miembro de la International society of orthomolecular medicine, ISOM.
- Miembro de la Asociaci├│n americana de medicina avanzada, ACAM
- Miembro de la Asociaci├│n m├®dica brasile├▒a de pr├Īctica ortomolecular AMBO y la Fapes
- Actual Presidente de la Sociedad Espa├▒ola de Nutrici├│n y Medicina Ortomolecular (SENMO)
- Director m├®dico de la cl├Łnica Cellmedik, Tenerife, Espa├▒a
- Director m├®dico de la Unidad de medicina anti envejecimiento y medicina integrativa en el hospital Virgen de la paloma, Madrid, Espa├▒a.
ŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗŌĆŗ
Reservados todos los derechos ┬®. Queda prohibida la reproducci├│n, parcial o total del contenido bajo cualquier forma sin el consentimiento previo y por escrito de Cien por Cien Natural SL. Si desea compartir la informaci├│n, se permite la reproducci├│n citando a Cien por Cien Natural SL o utilizando el link de su web. Cien por Cien Natural SL no se responsabiliza de uso indebido del contenido del art├Łculo.







